Toma de decisiones clínicas basadas en pruebas científicas
EVIDENCIAS EN PEDIATRÍA
Junio 2015. Volumen 11. Número 2
| La vitamina D en las otitis de repetición: ¿protagonista o intrusa?
Valoración: 0 (0 Votos)Autores: Ochoa Sangrador C, Rivas Fernández MÁ.
 Suscripción gratuita al boletín de novedades
Suscripción gratuita al boletín de novedades
Reciba periódicamente por correo electrónico los últimos artículos publicados
Suscribirse |
Autores:
Correspondencia:
Escenario Clínico
Pablito, de cinco años, sufre incontables otitis. Sus padres, alarmados, traen los resultados de una analítica que solicitó su otorrinolaringólogo: aunque las inmunoglobulinas son normales, el calcidiol (25-OH-D) es de 10 nmol/l (normal > 25 nmol/l). Quieren saber si suplementarlo con vitamina D ayudaría a evitar las recurrencias.
Usted les dice: "En los niños con infecciones de repetición está indicado descartar inmunodeficiencias, pero no entiendo en base a qué le han pedido el calcidiol. Sé que múltiples estudios asocian infecciones respiratorias con déficit de vitamina D; la controversia está en si esa disminución del calcidiol es causa o consecuencia de tantas infecciones y si tiene algún sentido suplementar a niños que viven tan cerca de la latitud 40°. Me documentaré”.
Para poder informar correctamente, se plantea las siguientes dudas clínicas:
Pregunta Clínica
(PICO)
Pregunta principal
¿En niños con otitis media de repetición [paciente], suplementar con vitamina D2 (ergocalciferol) o D3 (colecalciferol) [intervención] (no) [comparación] reduce el riesgo de recurrencias [outcome]?
Pregunta secundaria
¿En niños con infecciones respiratorias de repetición [paciente], analizar los niveles de 25-OH-D [intervención] (no) [comparación] permite predecir el riesgo de recurrencias[outcome]?
Comentario
Justificación: la vitamina D (VD) parece jugar un importante papel en la respuesta inmune a las infecciones, a través de mecanismos bioquímicos que se describen cada vez con mayor precisión (induce la formación de catelicidina LL-37, potente antimicrobiano endógeno)1,2. Pero, en base a los conocimientos actuales, ¿tiene sentido analizar el calcidiol o suplementar con VD a los niños para evitar la recurrencia de otitis, como algunos autores ya postulan hacer?3,4.
Al revisar la literatura científica surgen dudas que hacen cuestionar la validez del calcidiol como marcador de hipovitaminosis. Por ejemplo, ¿cómo es posible que en múltiples poblaciones lo “normal” sea que hasta el 89% de los niños sanos tengan niveles subóptimos?5-9, ¿no debería eso hacernos pensar que el punto de corte de calcidiol aceptado como válido (25-OH-D > 20 ngml) se debe reevaluar?10, ¿cómo se obtuvo esa cifra?11-14, ¿influye que existan diversos métodos de medición?15,16, ¿coinciden las definiciones de déficit intra/extraesquelético?17, ¿qué aporta la hormona paratiroidea?18, ¿no habría que buscar en la genética variables basales para cada etnia?19. Aún hay más resultados paradójicos sobre este parámetro: en un estudio de suplementación en neonatos, las dosis de VD que “normalizaban” el calcidiol les provocaba hipercalcemia, sugestiva de toxicidad20.
Lo cierto es que se están haciendo recomendaciones que no parecen sostenerse en pruebas sólidas. Por ejemplo Kazi21 recomienda suplementar con VD en base a su estudio descriptivo, sin grupo de control, tan solo porque confirma una asociación entre niveles deficientes de calcidiol e infecciones respiratorias de vías altas (IRVA). Si bien tanto él como la mayoría de losestudios observacionales llevados a cabo corroboran tal asociación entre niveles bajos de 25-OH-D y susceptibilidad a infecciones respiratorias22-25, se debe tener cautela: ¿eseste déficit causa de las infecciones, o su consecuencia? En este sentido, un dato con mucho peso es que los escasos ensayos clínicos llevados a cabo no consiguen, por el momento, demostrar que suplementar con VD modifique ni la incidencia ni la evolución clínica de las infecciones respiratorias26.
Llegados a este punto, con más de una docena de revisiones narrativas y sistemáticas que se citan unas a otras1,3,4,17,26-39 y tan solo un ensayo clínico sobre la eficacia de la VD en la otitis media40, se hace muy difícil interpretar la aplicabilidad de tan escasas pruebas en poblaciones concretas. Dicho de otro modo, parece que se ha escrito mucho, pero se ha investigado poco.
Para complicarlo más, no podemos olvidar que sobre el papel de la VD en la inmunidad influyen numerosos factores potencialmente modificadores del efecto, como la edad, época del año, latitud, etnia, nuestra situación nutricional respecto a otras vitaminas y oligoelementos, el agente responsable de la infección respiratoria, el órgano diana, etc.36,41,42.
Tampoco debemos subestimar el principioprimum non nocere, puesto que la VD no es inocua (página web de la Administración de alimentos y medicamentos de EE. UU., 2010). Se trata de una sustancia liposoluble, cuyo exceso se acumula en nuestra grasa; un consumo de dosis elevadas de manera rutinaria y muy prolongada podría interferir en la regulación que ejerce el gen Klotho sobre la homeostasis de los fosfatos a nivel de los fibroblastos34,39,43,44. Algunos no parecen creerlo. Así, en un ensayo clínico no finalizado aún45 se están administrando dosis de 2000 UI/día, sin tener en cuenta que la mayoría de los ensayos que utilizan dosis tan altas de VD no fueron diseñados para evaluar los daños a largo plazo28.
En este contexto, la pregunta que se plantea es si analizar el calcidiol para suplementar con VD a los niños que lo tengan bajo, con el objetivo de evitar la recurrencia de otitis en nuestra población, comporta mayor beneficio que riesgo.
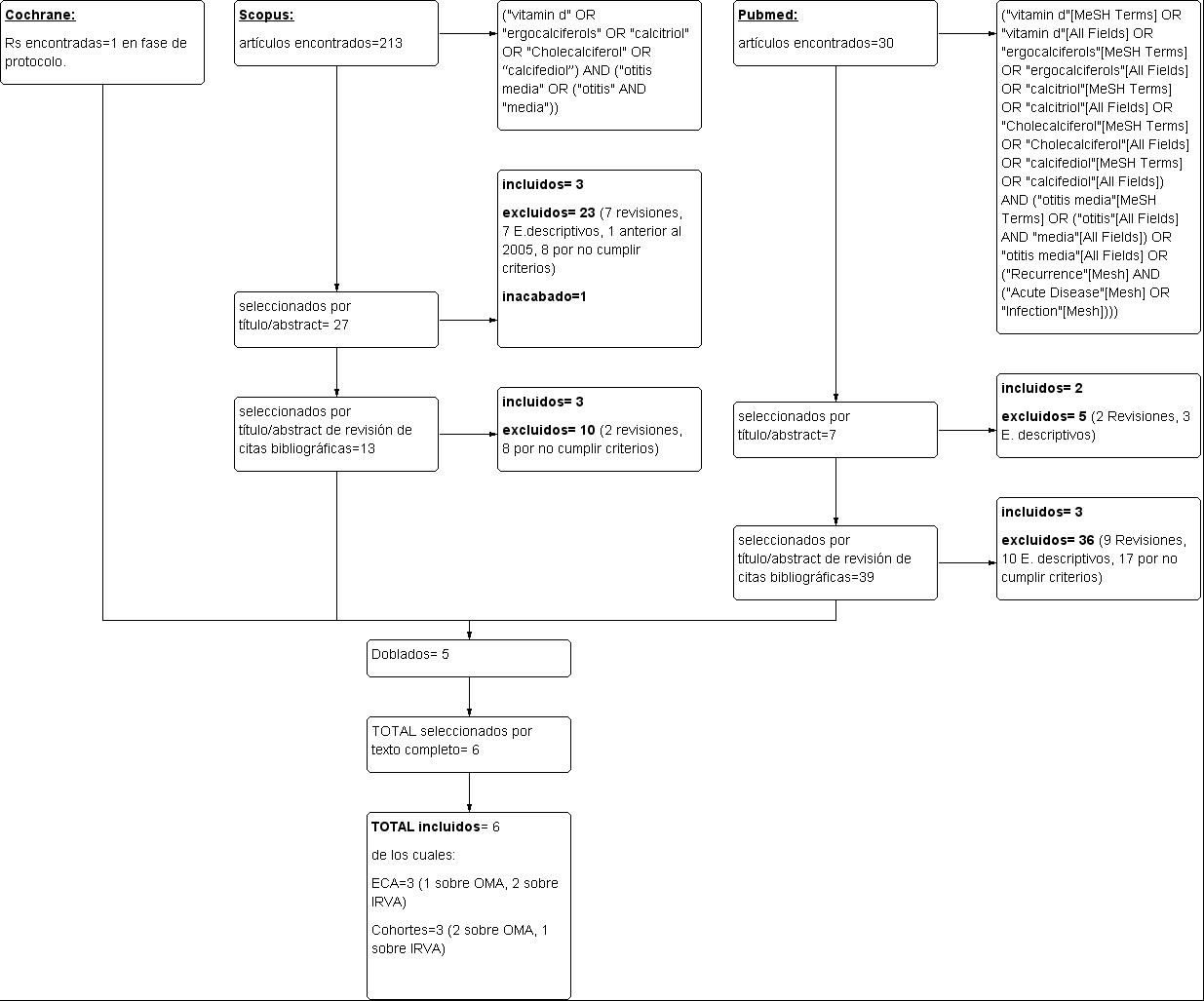
Evaluación crítica: se realizaron búsquedas por dos revisores independientes, en las bases de datos de PubMed, Scopus (incluye EMBASE) y Cochrane Collaboration. En la Figura 1se detallan las estrategias empleadas y los resultados.
Figura 1. Diagrama de flujo de los estudios incluidos en el análisis. Mostrar/ocultar
Criterios de selección: ensayos clínicos sobre eficacia de la suplementación con VD en la prevención de otitis o IRVA y estudios de cohortes sobre la VD como factor de riesgo o marcador de riesgo de otitis o IRVA. Otros diseños epidemiológicos no se incluyeron por no garantizar la secuencia exposición-efecto.
Criterios deexclusión: se excluyeron los llevados a cabo en adultos, los que aplicaban intervenciones múltiples (por ejemplo, polivitamínicos), los que evaluaban tan solo patología respiratoria de vías bajas (neumonías, asma, etc.), los estudios de casos y controles y los descriptivos. Las revisiones (narrativas o sistemáticas) no se incluyeron, pero se revisaron sus citas bibliográficas.
Resultados: sobre VD y otitis media en niños, se encontró un ensayo clínico40 y dosestudios de cohortes prospectivos8,24,resumidos en la Tabla 1.Se excluyeron dos estudios de casos y controles46,47 y uno descriptivo7. Sobre el tema hay publicadas también 16 revisiones narrativas o sistemáticas, de las que se han revisado sus citas bibliográficas, sin que añadiesen nuevos estudios. Respecto a la VD e IRVA, en general se han publicado dos ensayos clínicos48,49 y una cohorte prospectiva50,que se resumen en la Tabla 1. La heterogeneidad de los estudios no permite hacer un análisis agrupado.
Tabla 1. Estudios sobre otitis media aguda o infecciones de vías respiratorias altas. Mostrar/ocultar
En un ensayo clínico realizado en una pequeña muestra de niños con otitis recurrentes40, la suplementación con VD redujo en un 20% el riesgo de otitis (por cada cinco tratados se evitó una otitis). En otros dos ensayos clínicos48,49, diferentes tipos de suplementación han mostrado una reducción discreta del riesgo de gripe e infecciones respiratorias, sin que se describan efectos adversos.
En estudios de cohortes se ha encontrado que los escolares colombianos con niveles basales de VD < 50 nmol/l tenían un mayor riesgo de otitis (otalgia/otorrea con fiebre) que los que tenían > 75 nmol/l; pero estos, paradójicamente, presentaban mayor riesgo que aquellos con niveles intermedios24. Por otra parte, en una cohorte de recién nacidos coreanos8 no se encontraron diferencias en el riesgo de otitis enfunción de los niveles de VD (< 25 nmol/l, respecto a 25-75 y ≥ 75). Con estos mismos puntos de corte, en otra cohorte neozelandesa de recién nacidos50, sí se encontró un mayor riesgo de infecciones respiratorias con niveles < 25 nmol/l, pero solo respecto a los que tenían ≥ 75 nmol/l.
Conclusión: la calidad de la evidencia sobre la eficacia de la suplementación con VD para prevenir otitis se sustenta en un solo ensayo de pequeño tamaño muestral. Aunque otros dos ensayos aportan evidencia indirecta sobre eficacia en otras infecciones respiratorias, las dudas sobre el papel de la VD en el riesgo infeccioso hacen que debamos ser prudentes antes de generalizar la recomendación de suplementar a los niños con otitis recurrentes.
Con respecto a la decisión de realizar determinación de VD en los niños con otitis recurrentes, no hemos encontrado ningún estudio que haya evaluado su utilidad. En el ensayo clínico de Marchisio, los niveles alcanzados con la suplementación mostraban una clara relación dosis-efecto, sin embargo en los estudios de cohortes disponibles la información es contradictoria. Si hacemos un balance de beneficios y riesgos, el grupo de pacientes que más podrían beneficiarse de la determinación de niveles y de la suplementación serían los que presentan niveles < 25 nmol/l.
Resolución del escenario clínico: no tenemos evidencia suficiente para recomendar la determinación de VD en los niños con otitis recurrentes, tampoco para recomendar la suplementación rutinaria a todos estos niños. Sin embargo, sería aceptable que a aquellos a los que se les va a hacer un estudio analítico, como despistaje de inmunodeficiencias, se les ofreciera la determinación de 25-OH-D. En el caso de tener niveles < 25 nmol/l se les indicaría suplementación a dosis media, informando de las dudas sobre la eficacia. Quedaría por aclarar si hay bioequivalencia entre ergocalciferol (D2) y colecalciferol (D3)51 y la dosis de VD más eficaz y segura.
Cómo citar este artículo
Ochoa Sangrador C, Rivas Fernández MA. La vitamina D en las otitis de repetición: ¿protagonista o intrusa?. Evid Pediatr. 2015;11:20.
Bibliografía
- Bartley J. Vitamin D, innate immunity and upper respiratory tract infection. J Laryngol Otol. 2010;124:465-9.
- Van der Does AM, Bergman P, Agerberth B, Lindbom L. Induction of the human cathelicidin LL-37 as a novel treatment against bacterial infections.J Leukoc Biol. 2012;92:735-42.
- Borrella E, Hesher G, Israeli E, Shoenfeld Y. Vitamin D: a new anti-infective agent? Ann N Y Acad Sci. 2014;1317:76-83.
- Marchisio P, Nazzari E, Torretta S, Esposito S, Principi N. Medical prevention of recurrent acute otitis media: an update overview. Expert Rev Anti Infect Ther. 2014;12:611-20.
- Bellone S, Esposito S, Giglione E, Genoni G, Fiorito C, Petri A, et al. Vitamin D levels in a paediatric population of normal weight and obese subjects. J Endocrinol Invest. 2014;37:805-9.
- Bener A, Al-Ali M, Hoffmann GF. Vitamin D deficiency in healthy children in a sunny country: associated factors. Int J Food Sci Nutr. 2009;60:60-70.
- Linday LA, Shindledecker RD, Dolitsky JN, Chen TC, Holick MF. Plasma 25-hydroxyvitamin D levels in young children undergoing placement of tympanostomy tubes.Ann Otol Rhinol Laryngol. 2008;117:740-4.
- Shin YH, Yu J, Kim KW, Ahn K, Hong SA, Lee E, Yang SI, et al. Association between cord blood 25-hydroxyvitamin D concentrations and respiratory tract infections in the first 6 months of age in a Korean population: a birth cohort study (COCOA).Korean J Pediatr. 2013;56:439-45.
- Vierucci F, Del Pistoia M, Fanos M, Gori M, Carlone G, Erba P, et al. Vitamin D status and predictors of hypovitaminosis D in Italian children and adolescents: a cross-sectional study. Eur J Pediatr. 2013;172:1607-17.
- AlonsoMA, PallaviciniZF, RodríguezJ, AvelloN, Martínez-CamblorP, SantosF. Can vitamin D status be assessed by serum 25OHD in children? Pediatr Nephrol. 2015;30:327-32.
- Grant CC, Stewart AW, Scragg R, Milne T, Rowden J, Ekeroma A, et al. Vitamin D during pregnancy and infancy and infant serum 25-hydroxyvitamin D concentration.Pediatrics. 2014;133:e143-53.
- Bischoff-Ferrari HA, Giovannucci E, Willett WC, Dietrich T, Dawson-Hughes B. Estimation of optimal serum concentrations of 25-hydroxyvitamin D for multiple health outcomes. Am J Clin Nutr. 2006;84:18-28.
- Wicherts IS, Van Schoor NM, Boeke AJP, Lips P. Vitamin D deficiency and neuromuscular performance in the Longitudinal Aging Study Amsterdam (LASA). J Bone Miner Res. 2005;20:S35.
- Lips P, Pluijm SMF, Smit JH, Van Schoor NM. Vitamin D status and the threshold for secondary hyperparathyroidism in the longitudinal aging study Amsterdam (LASA). Bone. 2005;36:S141.
- Holick MF. Vitamin D status: measurement, interpretation, and clinical application. Ann Epidemiol. 2009;19:73-8.
- Hollis BW. Measuring 25-hydroxyvitamin D in a clinical environment: challenges and needs. Am J Clin Nutr. 2008;88:507S-10S.
- Shaw NJ, Mughal MZ. Vitamin D and child health: part 2 (extraskeletal and other aspects). Arch Dis Child. 2013;98:368-72.
- Valcour A, Blocki F, Hawkins DM. Effects of age and serum 25-OH-Vitamin D on serum parathyroid hormone levels. J Clin Endocrinol Metab. 2012;97:3989-95.
- Martineau AR, Jolliffe DA. Genetic variants modifying the influence of vitamin D.JAMA. 2013;309:872-3.
- Gallo S, Comeau K, Vanstone C, Agellon S, Sharma A, Jones G, et al. Effect of different dosages of oral vitamin D supplementation on vitamin D status in healthy, breastfed Infants. A randomized trial. JAMA. 2013;309:1785-92.
- Kazi M, Aamir K, Rana M, Farooq MA. Frequency of vitamin D3 deficiency in children presenting with frequent sino-pulmonary infections. Pak Paediatr J. 2013;37:101-5.
- Aydın S, Aslan I, Yıldız I, Ağaçhan B, Toptaş B, Toprak S, et al. Vitamin D D levels in children with recurrent tonsillitis.Int J Pediatr Otorhinolaryngol. 2011;75:364-7.
- Science M, Maguire JL, Russell ML, Smieja M, Walter SD, Loeb M. Low serum 25-hydroxyvitamin D level and risk of upper respiratory tract infection in children and adolescents.Clin Infect Dis. 2013;57:392-7.
- Thornton K, Marin C, Mora-Plazas M, Villamor E. Vitamin D deficiency associated with increased incidence of gastrointestinal and ear infections in school-age children 2013. Pediatr Infect Dis J. 2013;32:585-93.
- Yildiz I, Unuvar E, Zeybek U, Toptas B, Cacina C, Aydin S, et al. The role of vitamin D in children with recurrent tonsillopharyngitis.Ital J Pediatr. 2012;38:25.
- Autier P, Boniol M, Pizot C, Mullie P. Vitamin D status and ill health: a systematic review. Lancet Diabetes Endocrinol. 2014;2:76-89.
- Bergman P, Lindh AU, Bjorkhem-Bergman L, Lindh JD. Vitamin D and respiratory tract infections: a systematic review and meta-analysis of randomized controlled trials. PLoS One. 2013;8:e65835.
- Cranney A, Horsley T, O'Donnell S, Weiler H, Puil L, Ooi D. Effectiveness and safety of vitamin D in relation to bone health. Evid Rep Technol Assess. 2007;158:1-235.
- Charan J, Goyal JP, Saxena D, Yadav P. Vitamin D for prevention of respiratory tract infections: a systematic review and meta-analysis. J Pharmacol Pharmacother. 2012;3:300-3.
- Das R, Singh M, Panigrahi I, Naik S. Vitamin D supplementation for the treatment of acute childhood pneumonia: a systematic review. ISRN Pediatr. 2013;2013:459160.
- Elemraid MA, Mackenzie IJ, Fraser WD, Brabin BJ. Nutritional factors in the pathogenesis of ear disease in children: a systematic review.Ann Trop Paediatr. 2009;29:85-99.
- Esposito S, Baggi E, Bianchini S, Marchisio P, Principi N. Role of vitamin D in children with respiratory tract infection.Int J Immunopathol Pharmacol. 2013;26:1-13.
- Feleszko W, Ruszczynski M, Zalewski BM. Non-specific immune stimulation in respiratory tract infections. Separating the wheat from the chaff. Paediatr Respir Rev. 2014;15:200-6.
- Glade MJ. Vitamin D: Health Panacea or false Prophet? Nutrition. 2013:29:37-41.
- Jolliffe DA, Griffiths CJ, Martineau AR. Vitamin D in the prevention of acute respiratory infection: systematic review of clinical studies.J Steroid Biochem Mol Biol. 2013;136:321-9.
- Linday L, Umhau J, Shindledecker R, Dolitsky J, Holick M. Cod liver oil, the ratio of vitamins A and D, frequent respiratory tract infections, and vitamin D deficiency in young children in the United States. Ann Otol Rhinol Laryngol. 2010;119:64-70.
- Mao S, Huang S. Vitamin D supplementation and risk of respiratory tract infections: a meta-analysis of randomized controlled trials.Scand J Infect Dis. 2013;45:696-702.
- Theodoratou E, Tzoulaki I, Zgaga L, Ioannidis JP. Vitamin D and multiple health outcomes: umbrella review of systematic reviews and meta-analyses of observational studies and randomised trials. BMJ 2014;348:g2035.
- Walker VP, Modlin RL. The vitamin D connection to pediatric infections and immune function.Pediatr Res. 2009;65:R106-13.
- Marchisio P, Consonni D, Baggi E, Zampiero A, Bianchini S, Terranova L, et al. Vitamin D supplementation reduces the risk of acute otitis media in otitis-prone children.Pediatr Infect Dis J. 2013;32:1055-60.
- Abrams SA, Griffin IJ, Hawthorne KM, Gunn SK, Gundberg CM, Carpenter TO. Relationships among vitamin D levels, parathyroid hormone, and calcium absorption in young adolescents. J Clin Endocrinol Metab. 2005;90:5576-81.
- Tolppanen AM, Fraser A, Fraser WD, Lawlor DA. Risk factors for variation in 25-hydroxyvitamin D3 and D2 concentrations and vitamin D deficiency in children. Clin Endocrinol Metab. 2012;97:1202-9.
- Jones G. Pharmacokinetics of vitamin D toxicity. Am J Clin Nutr. 2008;88:582S-6S.
- Vanstone MB, Oberfield SE, Shader L. Hypercalcaemia in children receiving pharmacological doses of Vitamin D. Pediatrics. 2012;129:1060-3.
- Maguire JL, Birken C, Loeb M, Mamdani M, Thorpe K, Hoch J. Vitamin D Outcomes and Interventions in Toddlers - a TARGet Kids! randomized controlled trial. BMC Pediatrics. 2014;14:37.
- Cayir A, Turan MI, Ozkan O, Cayir Y, Kaya A, Davutoglu S, et al. Serum vitamin D levels in children with recurrent otitis media.Eur Arch Otorhinolaryngol. 2014;271:689-93.
- Elemraid MA, Mackenzie IJ, Fraser WD, Harper G, Faragher B, Atef Z, et al. A case-control study of nutritional factors associated with chronic suppurative otitis media in Yemeni children. Eur J Clin Nutr. 2011;65:895-902.
- Urashima M, Segawa T, Okazaki M, Kurihara M, Wada Y, Ida H. Randomized trial of vitamin D supplementation to prevent seasonal influenza A in schoolchildren. Am J Clin Nutr. 2010;91:1255-60.
- Camargo C, Ganmaa D, Frazier L, Kirchberg F, Stuart J, Kleinman K, et al. Randomized trial of vitamin D supplementation and risk of acute respiratory infection in Mongolia. Pediatrics. 2012;130:e561-7.
- Camargo C, Ingham T, Wickens K, Thadhani R, Crane K, Epton M, et al. Cord-blood 25-hydroxyvitamin D levels and risk of respiratory infection, wheezing, and asthma. Pediatrics 2011;127:e180-7.
- Gallo S, Phan A, Vanstone CA, Rodd C, Weiler HA. The change in plasma 25-hydroxyvitamin D did not differ between breast-fed infants that received a daily supplement of ergocalciferol or cholecalciferol for 3 months. J Nutr. 2013;143:148-53.


Envío de comentarios a los autores